![]()
Objectif : déterminer le débit d'un cours d'eau en évaluant sa section et en mesurant sa vitesse.
A.1.1. Détermination de la section du cours d'eau
Diviser la largeur de la rivière
en intervalles réguliers de 0,5 ou 1 m.
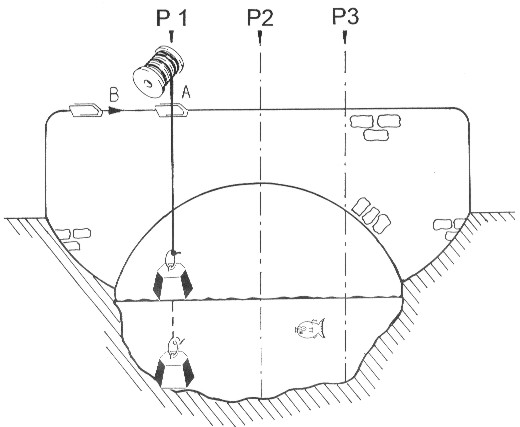
Si l'on peut utiliser un pont, indiquer ces intervalles sur le parapet.
Attacher un poids à une ficelle et le laisser descendre jusqu'à la surface de l'eau. Prendre une hauteur de repère fixe sur le pont et placer une attache sur la ficelle à cette hauteur. Laisser descendre le poids jusqu'au fond de la rivière et placer une seconde attache sur la ficelle en face du point de repère.
Mesurer la distance entre les 2 attaches pour obtenir la profondeur de la rivière.
Répéter l'opération pour couvrir toute la largeur de la rivière.S'il n'y a pas de pont et si la rivière est peu profonde, on peut tendre une corde horizontalement entre les 2 berges et mesurer la profondeur à l'aide d'un double mètre pliant en respectant les mêmes intervalles.
La section de la rivière peut être représentée par une succession de trapèzes.
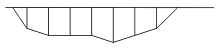
L'aire de cette section vaut approximativement : S = l . Pm
" l " est la largeur de la rivière et " Pm " est la profondeur moyenne obtenue en divisant la somme de toutes les profondeurs mesurées par le nombre de mesures.
(si nécessaire, un calcul plus précis de la section peut être effectué en utilisant une formulation mathématique plus élaborée)
A.1.2. Détermination de la vitesse
Repérer 2 limites séparées de quelques mètres sur le cours de la rivière : les 2 parapets d'un pont ou 2 cordes tendues au-dessus de l'eau. Mesurer la distance L qui les sépare. Lâcher un bloc de bois en amont et mesurer avec un chronomètre le temps nécessaire pour passer d'une limite à l'autre. Effectuer la mesure plusieurs fois en lâchant le bloc à des endroits différents pour obtenir un temps moyen Tm.
Calculer la vitesse moyenne : v = L / Tm
Mesure du débitLe volume d'eau qui s'écoule pendant le temps moyen Tm est donné par le produit de la section S par la distance L séparant les 2 limites V = S . L.
Le débit est le volume écoulé par unité de temps : D = V / T .Date :
Nom du cours d'eau : .
Commune : ..
|
Symbole
|
Formule
|
Réponse
|
||
| Longueur |
L
|
..
|
m
|
|
| Largeur |
I
|
..
|
m
|
|
| Profondeur | 1ère |
P1
|
..
|
m
|
| 2ème |
P2
|
..
|
m
|
|
| 3ème |
P3
|
..
|
m
|
|
| 4ème |
P4
|
..
|
m
|
|
| 5ème |
P5
|
....
|
m
|
|
| 6ème |
P6
|
..
|
m
|
|
| Profondeur moyenne |
Pm
|
(P1+P2+P3+P4+P5+P6)/6
|
m
|
|
| Temps | 1er |
T1
|
..
|
s
|
| 2ème |
T2
|
..
|
s
|
|
| 3ème |
T3
|
..
|
s
|
|
| Temps moyen |
Tm
|
(T1+T2+T3)/ 3
|
s
|
|
| Vitesse |
v
|
L / Tm
|
m/s
|
|
| Volume d'eau |
V
|
L x I x Pm
|
m3
|
|
| Débit |
D
|
V / Tm
|
m3/s
|
|
![]()
Le repérage de la température s'effectue dans la rivière au moyen d'un thermomètre approprié.
La température exerce son influence sous 2 aspects principaux :
Elle modifie la solubilité des gaz dans l'eau
Exemple : solubilité de l'O2 atmosphérique dans l'eau douce à différentes températures :
| T (°C) | Conc. O2 (mg/l) |
. | T (°C) | Conc. O2 (mg/l) |
. | T (°C) | Conc. O2 (mg/l) |
. | T (°C) | Conc. O2 (mg/l) |
| 0 | 14,6 | . | 7 | 12,2 | . | 14 | 10,4 | . | 21 | 9,0 |
| 1 | 14,2 | . | 8 | 11,9 | . | 15 | 10,2 | . | 22 | 8,9 |
| 2 | 13,8 | . | 9 | 11,6 | . | 16 | 10,0 | . | 23 | 8,7 |
| 3 | 13,5 | . | 10 | 11,3 | . | 17 | 9,8 | . | 24 | 8,6 |
| 4 | 13,1 | . | 11 | 11,1 | . | 18 | 9,6 | . | 25 | 8,4 |
| 5 | 12,8 | . | 12 | 10,9 | . | 19 | 9,4 | . | 26 | 8,2 |
| 6 | 12,5 | . | 13 | 10,6 | . | 20 | 9,2 | . | 27 | 8,1 |
La température modifie la vitesse des réactions chimiques et biochimiques
Lorsque la température s'élève, les bactéries consomment plus de dioxygène, ce qui réduit la quantité disponible pour les autres êtres vivants de l'écosystème.
A.2.2. La conductivité électrique
La conductivité se mesure à l'aide d'un conductivimètre.
Elle s'exprime en mS/cm (microsiemens par cm).
Elle est caractéristique du nombre total d'ions présents dans la solution.
Il se mesure à l'aide d'un pH-mètre de poche. Celui-ci doit être maintenu dans l'eau un temps suffisant pour indiquer une valeur stable. Il devrait être calibré avant la mesure en utilisant une solution tampon.
Le pH influence la dissolution des roches et la précipitation de certains sels.
Le pH influence fortement la production de certaines plantes et le maintien d'autres organismes vivants dans la rivière.
Le pH est important dans les rivières pauvres en carbonates dont le pouvoir tampon est très faible. Elles sont donc plus sensibles aux apports extérieurs d'un pH différent.
Le pH est aussi important dans les rivières déficientes en dioxygène : la dégradation des molécules organiques s'arrête souvent au stade d'acides organiques.
Rôle du dioxygène dans l'eau :
Le dioxygène a une position centrale dans l'écosystème. Lorsque l'oxygène se raréfie, les conditions de vie deviennent défavorables pour beaucoup d'animaux : bactéries, unicel-lulaires, poissons...
Une pollution organique, qui a pour effet de faire baisser le taux d'oxygène de la rivière, se traduit par l'élimination rapide des espèces exigeantes en oxygène (larves d'éphémères, truites...), puis par un appauvrissement progressif de la faune et de la flore pour aboutir à un écosystème composé uniquement d'espèces tolérantes.
Echange avec l'atmosphère :
La quantité de dioxygène échangée avec l'atmosphère dépend de la température, de la surface d'eau en contact avec l'air par rapport au volume de la rivière et de la turbulence du courant.
Consommation et production de dioxygène par l'écosystème :
La consommation de dioxygène dépend des animaux, des poissons, des bactéries actives... présents dans la rivière tandis que la production par photosynthèse dépend de la luminosité arrivant sur les algues ou plantes vertes, donc de l'exposition au soleil et de la turbidité de l'eau.
Analyse immédiate et DBO5 :
L'analyse au bord de la rivière permet de déterminer la quantité de dioxygène dissous dans l'eau de la rivière à l'instant du prélèvement. Celle-ci s'exprime en mg/l. Il est toutefois utile de tenir compte de la température de l'eau et d'exprimer aussi cette concentration en pourcentage de la concentration maximale indiquée dans le tableau.
En complément, on peut mesurer la quantité de dioxygène subsistant après cinq jours dans un échantillon gardé en flacon fermé et à l'obscurité. Par différence, on détermine ainsi la demande biologique en oxygène sur cinq jours DBO5. Celle-ci permet d'estimer la quantité de bactéries et d'unicellulaires présents dans l'eau.
Dosage du dioxygène par le coffret Merck :
Le dosage du dioxygène peut être effectué par la méthode de Winkler, basée sur des réactions d'oxydo-réduction.
En milieu alcalin, l'oxygène dissous réagit quantitativement avec l'hydroxyde de manganèse (II) :MnSO4 + 2 KOH
Mn(OH)2
+ K2S04
Mn(OH)2+ 1/2 O2
MnO2.H2O
En milieu acide, le dioxyde de manganèse hydraté réagit avec un iodure pour libérer de l'iode :
MnO2.H2O + 2 KI + 2 H2SO4
MnSO4 + K2SO4 + 3 H2O + I2
Le diiode libéré est dosé par une solution titrée de thiosulfate de sodium en présence d'amidon :
I2 + 2 Na2SO3
2 NaI + Na2S4O6.
Remarque : lors de l'addition de H2SO4, les nitrites qui perturbent ce titrage peuvent être détruits par de l'azoture de sodium
2 HNO2 + 2 NaN3 + H2SO4Na2SO4 + 2 N2 + 2 N2O + 2 H2O
Mode d'emploi
1. Rincer le flacon en verre, dans lequel se trouvent quatre billes en verre, plusieurs fois avec de
l'eau à examiner et le remplir, jusqu'à débordement.
2. Ajouter successivement cinq gouttes de Réactif 1 et cinq gouttes de Réactif 2. Fermer le flacon
avec le bouchon en verre biseauté, bien agiter et laisser reposer pendant une minute à l'état fermé.
3. Ajouter dix gouttes de Réactif 3, refermer et bien agiter à nouveau.
4. Rincer le récipient à essais avec la solution ainsi obtenue et le remplir jusqu'au repère
(correspondant à 5 ml).
5. Ajouter une goutte de Réactif 4 et agiter. Selon la teneur en oxygène, la solution se colore en une
teinte allant du violet au bleu.
6. Poser simplement le dispositif de titrage et le remplir avec le Réactif 5 (solution de titrage) en
tirant lentement la seringue, jusqu'à ce que le bord inférieur du joint noir coïncide avec le 0 de
l'échelle mg/l d'oxygène.
7. Sortir la pipette de titrage et frotter brièvement la pointe du tube sur le bord du flacon. A l'échantillon d'eau
préparé, ajouter alors la solution de titrage goutte à goutte, jusqu'à ce que la couleur de l'échantillon d'eau
vire du bleu à l'incolore.
8. Lire la teneur en oxygène de l'eau en mg/l sur l'échelle de la pipette de titrage.
9. Lorsque l'analyse est terminée, pousser le piston de la pipette de titrage vers le bas et visser
solidement cette dernière sur le flacon de réactifs.
| Type de roches | Argileuse | Siliceuse | Calcareuse Réaction à l'acide |
Carbonée | Conglomératique | |
|
Consolidation croissante
|
Roches meubles | ARGILE Colle sur la langue. Etat humide : compacte et malléable . Etat sec : se fissure; se désagrège facilement en une fine poussière. |
SABLE Crisse sous la dent. Grains visibles à l'il nu ou avec une faible loupe. |
Débris animaux contenant
du calcium (squelettes, coquilles
)
OU Précipités de carbonates de Calcium. |
Débris |
GRAVIER Grains de plus de 2 mm de diamètre. |
| SCHISTE
Les cailloux de schiste sont plats et feuilletés sur la tranche. Le canif peut assez facilement détacher des feuillets. L'ongle peut le rayer. |
GRES
Raye le verre (même composition : silice : SiO2). On peut détacher les grains de sable avec le canif. |
CRAIE CALCAIRE Couleur grise Ne raye pas le verre. |
CHARBON Couleur noire. Tache les doigts. |
POUDINGUE
Sorte de gravier, compacté (éléments constitutifs soudés les uns aux autres) ou "cimenté" (enrobés par une pâte durcie). |
||
| Roches métamorphiques | ARDOISE
(ou phyllade) Les cailloux d'ardoise sont encore plus plats. On ne sait plus détacher les feuillets. L'ongle sait toujours rayer |
QUARTZITE
Raye le verre. On ne sait pas détacher les grains, car ils sont littéralement soudés les uns aux autres. |
MARBRE
Couleurs variées. Aspect décoratif lorsque poli. Ne raye pas. |
ANTHRACITE Idem, mais plus compact et aspect brillant. |
Poudingue métamorphique Idem |
|
| Autres
Roches |
... | SILEX (SiO2
précipité) Raye le verre. Toucher soyeux sur les faces; coupant sur les tranches. |
... | Graphite et diamant (carbone pur : ne sont plus des roches mais des minéraux). | ... | |
Consignes pour la reconnaissance des roches sédimentaires belges
Remarque : les roches endogènes, qu'elles soient volcaniques ou magmatiques, sont extrêmement rares en Belgique, ce qui limite la reconnaissance aux roches sédimentaires.
![]() Matériel nécessaire
Matériel nécessaire
· Un marteau pour prélever les roches en place;
· Une plaque de verre pour le test de la rayure des roches siliceuses;
· Un canif (test des grains pour le grès ou test des feuillets pour les schistes);
· Un peu d'acide dilué pour le test des carbonates;
· Une loupe pour distinguer les grains constitutifs des sables, des grès ou des quartzites;
· Petits sachets plastique type congélation et marqueur indélébile pour le stockage des échantillons.
| Les échantillons de roche cohérente doivent toujours provenir de roches "en place" ; ils ne peuvent en aucun cas être de simples cailloux ramassés par terre ou dans le lit d'un cours d'eau. |
![]() En résumé
En résumé
Roches meubles
Les critères de reconnaissance sont essentiellement visuels et tactiles
Roches cohérentes
Les critères de reconnaissance sont essentiellement la dureté (tests de rayure - rayure du verre ou rayure par l'ongle) et la réactivité à l'acide.
La couleur n'est jamais un critère déterminant pour les roches argileuses et siliceuses ; elle peut par contre être invoquée pour la craie, le calcaire, les charbons et les marbres (à condition que les échantillons soient propres).
![]() Remarque importante
Remarque importante
On rencontre fréquemment des roches de composition mixte. Exemples :
· Grès calcareux
· Schistes calcareux
· Schistes gréseuxEn croisant les critères, on peut cependant toujours obtenir une détermination fiable.
![]() Où trouver ces différentes roches ?
Où trouver ces différentes roches ?
· On peut trouver les roches meubles (sable, argile et gravier) dans le lit des cours d'eau
(Ourthe et Blanc Gravier).
· On trouvera des grès ou des quartzites dans les bancs de roches affleurantes sur les
bords du ruisseau du Blanc Gravier.
· Les falaises du lieu-dit Rochers du Bout du Monde sont constituées de calcaire.
· La tranchée de la bretelle d'autoroute montre des affleurements de quartzites et de schistes.